Actualité Sciences:Physiologie du GLP-1 dans l'homéostasie postprandiale du glucose :
Mots clé: GLP-1, GIP, incrétine, diabète type 2, actualité, glycémie post prandiale.
* Les hormones incrétines peuvent être responsables de jusqu'à 70% de la sécrétion d'insuline post-prandiale.
* La GLP-1 est une petite molécule qui peut traverser la barrière
hémato-encéphalique et agir sur le système nerveux central pour promouvoir la
satiété.
Chez les individus sains, la glycémie à jeun est
principalement influencée par les effets de l'insuline et le glucagon. Cependant,
en post-prandial, la situation est tout
à fait différente vu que les incrétines jouent un rôle primordial.
Après l'ingestion
d'un repas, les incrétines GLP-1 (glucagon-like peptide 1) et le GIP (glucose-dependent
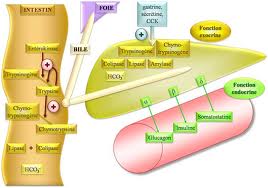
insulinotropic polypeptide), sont sécrétées par l'intestin. Cela se traduit par :
* une sécrétion d'insuline glucose-dépendante par le
pancréas.
*une diminution de la sécrétion de glucagon par le foie.
*un ralentissement de la vidange gastrique.
* suppression de
l'appétit.
Cet article passera en revue la physiologie du GLP-1 et
son rôle de premier ordre dans l'homéostasie de la glycémie postprandiale.
«L’effet incrétine», phénomène par lequel l'augmentation des
taux d'insuline en réponse au défi du glucose est significativement plus élevée
lorsque le glucose est administré par voie orale par rapport à une dose
intraveineuse unique, illustre le rôle clé de l'intestin et des hormones
incrétines dans la régulation glycémique en période postprandiale.
2 L'implication est que ce n'est pas seulement la quantité
de glucose qui pénètre dans la circulation seule qui régit la sécrétion de
l'insuline... En effet, des études ont démontré que la sécrétion d'insuline en
fonction de l'incrétine peut être responsable de 50% à 70% d'insuline totale
sécrétée en réponse à une charge orale de glucose.
Les incrétines
semblent exercer leurs effets seulement, lorsque le glucose sérique est élevé
au-dessus 0.4. En plus de son rôle essentiel de stimuler la sécrétion
d'insuline par le pancréas (en post-prandial), le GLP-1 a également d’autres effets notables sur les autres organes et
tissus ;
Dans le foie, le
GLP-1 inhibe la sécrétion du glucagon.
Au niveau de
l'estomac, le GLP-1 retarde la vidange gastrique et favorise la satiété permettant
de réduire l'apport calorique et ainsi le poids.
On croit que les mécanismes de la vidange gastrique et à la satiété sont
doubles:
La GLP-1 peut agir directement sur l'estomac lui-même,
provoquant une distension gastrique et une sensation de plénitude.
Par ailleurs, vu que le GLP-1 est une petite molécule qui
peut traverser librement la barrière hémato-encéphalique, la satiété peut être
médiée par le système nerveux central…
En combinaison avec
du glucose, le GLP-1 stimule la production d'insuline par les cellules bêta. Dans
des études animales, il aurait été montré que le GLP-1 augmente la masse des cellules
« bêta » du pancréas, par augmentation de la bêta-prolifération
cellulaire, ainsi qu'une diminution de l’apoptose de ces dernières. Il a également
été démontré qu'elle affecte la sensibilité à l'insuline, médiée par le SNC et
l'absorption du glucose dans le muscle et le tissu adipeux.
Comme pour toute hormone, la quantité de GLP-1 circulante
est régie par l'élimination, ainsi que la sécrétion.
LeGLP-1 subit une dégradation rapide par l'enzyme DPP-4
(dipeptidyl peptidase-4) .Les preuves suggèrent l’existance d'autres mécanismes
d'élimination du GLP-1.
En résumé, les hormones incrétines GLP-1, et le GIP,
agissent par différents mécanismes, sur plusieurs systèmes organiques pour
augmenter la sécrétion d'insuline, retarder la vidange gastrique, promouvoir la
satiété, et causer une perte de poids. Par rapport à notre connaissance de
quelques dizaines d'années, ces découvertes représentent d'importants ajouts à
notre compréhension des mécanismes physiologiques complexes qui régissent
l'homéostasie du glucose en post-prandial chez les individus sains.
Article original en Anglais.
Source : medpagetoday
Article traduit par B.J.
References:
Freeman JS. Role of the Incretin Pathway in the Pathogenesis of Type 2 Diabetes Mellitus. Cleve Clin J Med. 2009;76(suppl 5):S12-S19.
Nauck MA, et al. Normalization of Fasting Hyperglycaemia by Exogenous Glucagon-Like Peptide 1 (7-36 Amide) in Type 2 (Non-Insulin-Dependent) Diabetic Patients. Diabetologia. 1993;36:741-744.
Vaag AA, et al. Gut Incretin Hormones in Identical Twins Discordant for Non-Insulin-Dependent Diabetes Mellitus (NIDDM)-Evidence for Decreased Glucagon-Like Peptide 1 Secretion During Oral Glucose Ingestion in NIDDM Twins. Eur J Endocrinol. 1996;135:425-432.
Toft-Nielsen MB, et al. Determinants of the Impaired Secretion of Glucagon-Like Peptide-1 in Type 2 Diabetic Patients. J Clin Endocrinol Metab. 2001;86:3717-3723.
Cernea S, et al. Therapy in the Early Stage: Incretins. Diabetes Care. 2011;34(suppl 2):S264-S271.
Freeman JS. A Physiologic and Pharmacological Basis for Implementation of Incretin Hormones in the Treatment of Type 2 Diabetes Mellitus. Mayo Clin Proc. 2010;85(suppl 12):S5-S14.








Votre article m'a tellement même si je lis rarement sur le net, le niveau de votre écriture m'a encouragé pour terminer la lecture,et c'est vraimenet à relire !!! bon courage !!
RépondreSupprimer